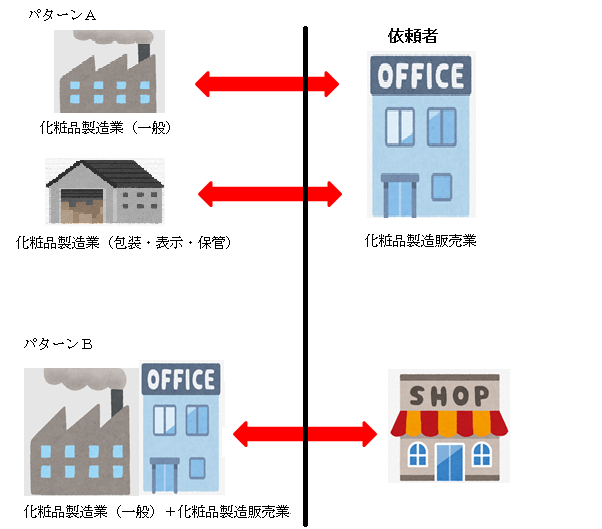
化粧品製造販売業の許可や化粧品製造業の許可は5年毎に更新しなければなりません。
更新時には更新申請を2ヶ月前までに行う必要があるのですが、
更新申請をする前に、更新時調査(実地調査)を受けておく必要があります。
(更新時調査(実地調査)が終了していないと、更新申請が出来ない場合もあります。)
更新時調査が終わってから、更新申請(FD申請を用いて)を行います。
各都道府県によりその受ける時期は違いますが、各都道府県薬務課等から更新時調査(実地調査)の日程調整の連絡が来ます。
更新時調査(実地調査)に不安が有る場合には、サポート支援いたしますので、お問い合わせから お願いします。
どのような調査が行われるのか?
ざっくりですが、下記のような内容になります。
1. 製造販売業許可申請、製造業許可申請の許可された内容に合致しているか?
どこの都道府県でも同じような内容の基本的な情報を記入する用紙が送られてくるのでそれに記入します。
・人的要件・・・化粧品製造販売業の総括製造販売者の氏名、住所、資格
品質保証責任者の氏名
安全管理責任者の氏名
化粧品製造業の責任技術者の氏名、住所、資格
・設備要件・・・化粧品製造業の設備状況
*上記は変更があった場合には30日以内に変更届を出さないといけませんので、最新の許可、届の内容と合っていないといけません。
この5年間の間に変更届などしている場合にその変更届や初回の許可申請書などの資料は保存されていますか?
(けっこう散逸している会社さんもありますので注意です)
2. 業務システム要件
・化粧品製造販売届、品質標準書が揃っているか?
販売品目一覧表のようなものを調査前に予め提出するところもあるようです。
この品目一覧に列挙された販売品目の製造販売届、品質標準書が全て揃っているかがチェックされます。
・化粧品GQP・・・GQP手順書のとおり業務が行われ、記録がされているか?
・化粧品GVP・・・GVP手順書のとおり業務が行われ、記録がされているか?
GQP、GVPについては、化粧品製造販売業者として行わなければならない業務 で書かれている内容の手順通りに行われ、その記録が整備されているかのチェックになります。
特に注意して頂きたいのは、
化粧品製造業の製造記録です。
化粧品製造販売業はGQP手順に従い、市場出荷判定を行いその記録を残しますが、
なにをもって判定したのかというエビデンスとして、化粧品製造業の製造記録が見られます。
製造は海外メーカーだから製造記録なんてありません、などと言わないようにしてください、
日本に入って来てからの包装・表示・保管を行った製造記録が必要になるのですから。
でないと、どんな法定表示を行ったのかとかわからないですよね。
GQP、GVPの業務についてはこの5年間の実績が調査されるわけですので
更新の前になってあわてて見直しても5年前の記録などはどうしようもありませんよね。
最低でも年1回の自己点検で
2016年7月28日化粧品製造販売業者が行う業務ー自己点検 で書いたように、自己点検して事前に問題点を判明させ、更新時の監査に耐えられるようにすべきです。
更新時調査が無事に終了しますと、更新申請を2ヶ月前までに化粧品製造販売業更新申請や化粧品製造業更新申請が行う事が出来ます。
更新申請は新規の許可申請と時と同じようにFD申請を行います。
更新時調査に不安が有るような場合には、サポート支援いたしますので、
お問い合わせから 質問して下さい。