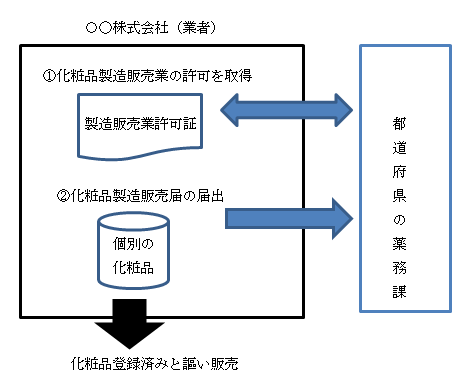
化粧品品質標準書は化粧品製造販売業の許可を取った会社(化粧品製造販売業者、元)が化粧品製造販売届を届出した販売名毎に作成する化粧品GQP(品質管理業務)で求められる社内文書(内部文書)です。
化粧品製造販売届を都道府県薬務課へ届出したら、可能な限り早急に社内文書として化粧品品質標準書を作成しましょう、弊社では化粧品品質標準書の作成を指導しています。
化粧品品質標準書の記載項目としては
1販売名
2製造販売の届出年月日
(医薬部外品の場合は承認番号、承認年月日)
輸入品の場合は輸入届出年月日等
3効能効果
4使用方法(用法用量等)及び使用上の注意事項
5製造所の名称、所在地及び許可番号
(外国製造所の場合は認定事項又は届出事項)
6原料成分の名称、規格及び配合量
7製造方法
(製造所が複数ある場合には製造所ごとに記載)
8容器、包装形態及び表示内容
9保管条件及び取扱い上の注意事項
10製品規格及び試験検査方法
11試験検査所の名称、所在地
12出荷基準
13製造業者等との取決め内容
14その他必要事項
このように、製造業(一般)で作成される製品標準書に比べれば作業内容が無いので至ってシンプルです
が、
各項目に何を書けば良いか分かりますでしょうか?
弊社では、
化粧品の品質標準書モデルひな形をテンプレートとして使え、何を書けば良いか記載例(書き方)を説明したをwordソースのものをこのサイトの化粧品手順書一式では提供し作成指導をしています、
また、
運用サポート有料会員様には化粧品品質標準書を作成していなかった場合には作成指導を行っています。
化粧品品質標準書は社内文書であり、行政等への提出(届出)が必要ないために作成していない
また、
化粧品品質標準書は各都道府県から公開されていますが、どのモデルひな型もexcel1枚の記載項目だけで記載例(書き方)項目毎にどのな内容を記載すれば良いのかは書かれていません
何を書けば良いのかが分からない状態のため経験のない化粧品製造販売業者さんは作成していない会社さんも多いでしょう。
弊社では、
化粧品の品質標準書モデルひな形をテンプレートとして使え、何を書けば良いか記載例(書き方)を説明したをwordソースのものをこのサイトの化粧品手順書一式では提供し作成指導をしています。
化粧品品質標準書の作成方法として書き方記載例を詳細説明したひな形になっています。

このサイトの手順書一式では化粧品の品質標準書モデルひな形テンプレートを提供しています
化粧品品質標準書は、化粧品製造販売業の更新調査(実地調査)で一番みられるところですが、
化粧品品質標準書が作成されていないという事で更新が出来ない事はありません、理由は法律的に品質標準書は必須ではないからです、ですので行政書士さんに製造販売届を委託しても品質標準書は作成してくれない行政書士さんもいるのです(更新時調査の時の薬務課さんの心証は悪くなるでしょうが・・・・)
ただ、このサイト的には化粧品品質標準書が作成されていないというのは、化粧品製造販売業者としては運用において致命的と考えています。
原材料、法定表示の内容、検査基準や検査方法、出荷判定や市場出荷判定など、など、など
全てはこの作成された化粧品品質標準書をもとに作業を行うのですから、
なにをもってそれを行ったのかのエビデンスとなるわけです。
もし、化粧品製造販売届は届出されているが化粧品品質標準書は作成していない会社さんがおられましたらご相談下さい。
ご自分で作成した化粧品品質標準書は
それを見て作業出来ますか?
それを見て出荷判定の方法が分かりますか?
それを見てどんな試験をするかわかりますか?
その品質標準書は関係者に周知されていますか?
その品質標準書は更新履歴(版数)管理されていますか?
など・・・・・全ての事が化粧品品質標準書を見ればわかるようにしなければなりません。
化粧品品質標準書を作るのは、「更新等で見られるから」というて考え方ではどうしてもなおざりになるでしょう。
その化粧品に関する情報を品質標準書に蓄積していくんです。
そうする事により、例えば担当者の引き継ぎにも簡単ですよね、立派な会社の資産です。
これらは、化粧品製造販売業の中で仕事した方でないと、実務運営経験が無いので難しい話ではありますので、
化粧品製造販売業者での経験者に指導を受けたりした方が良いと思います。
ただ一つ言える事は、品質標準書がA4で1枚で済むなんてことはあり得ませんから。
(どうしても、各都道府県のモデルひな形がExcelで1枚で出来ているために勘違いしてしまうようです。そこから別紙●●として膨らむんです)
不明点等ありましたら、お問い合わせから 質問して下さい。